国内上市的pd-1抑制剂
*** 次数:1999998 已用完,请联系开发者***

?^? ...肿瘤情报(第71期):信达生物PD-1抑制剂达伯舒在澳门特区获批上市;...2018年12月24日在中国大陆获批上市,目前已获批七项适应症,涵盖非鳞状非小细胞肺癌、鳞状非小细胞肺癌、EGFR突变非鳞状非小细胞肺癌、肝癌、胃癌、食管癌、霍奇金淋巴瘤。达伯舒®是唯一将五大高发瘤种一线治疗均纳入国家医保目录的PD-1抑制剂,也是中国首个且目前唯一...

21CC肿瘤情报(第55期):默沙东PD-1抑制剂帕博利珠单抗在华获批新...获批默沙东PD-1抑制剂帕博利珠单抗在华获批新适应证9月8日,默沙东宣布,其PD-1抑制剂帕博利珠单抗(商品名:可瑞达®)已获得中国国家药品... 本轮融资将为赛恩医疗首款获批上市的冷冻旋切活检系列产品的商业化以及在肿瘤早诊早治领域内的创新治疗产品研发提供资金与资源支持。...

...PARP抑制剂组合疗法;齐鲁制药PD-1/CTLA-4组合抗体新药申报上市该药品是首个结合PARP抑制剂与醋酸阿比特龙、具双重机制的口服片剂。齐鲁制药PD-1/CTLA-4组合抗体新药申报上市8月12日,CDE官网显示,齐鲁制药艾帕洛利单抗/托沃瑞利单抗(QL1706)注射液上市申请获受理。这是全球首个申报上市的PD-1/CTLA-4组合抗体。QL1706是齐鲁制...
康方生物B(09926.HK)依达方的新药上市申请获国家药监局批准【财华社讯】康方生物B(09926.HK)公布,中国国家药品监督管理局(“NMPA”)已批准公司自主研发的全球首创双特异性抗体新药依达方®(依沃西注射液,PD-1/VEGF)的新药上市申请,适应症为联合化疗用于治疗经表皮生长因子受体(“EGFR”)酪氨酸激霉抑制剂(“TKI”)治疗后进展的...

⊙﹏⊙‖∣° 国产第二款PD-1获FDA批准其PD-1抑制剂替雷利珠单抗上市,用于治疗既往经系统治疗后不可切除、复发性局部晚期或转移性食管鳞状细胞癌(ESCC)患者。这是继君实生物的特瑞普利单抗登陆美国市场后,第二款登陆美国市场的中国PD-1抑制剂。此外,这也是继泽布替尼后,百济神州第二款在美获批上市的产品。
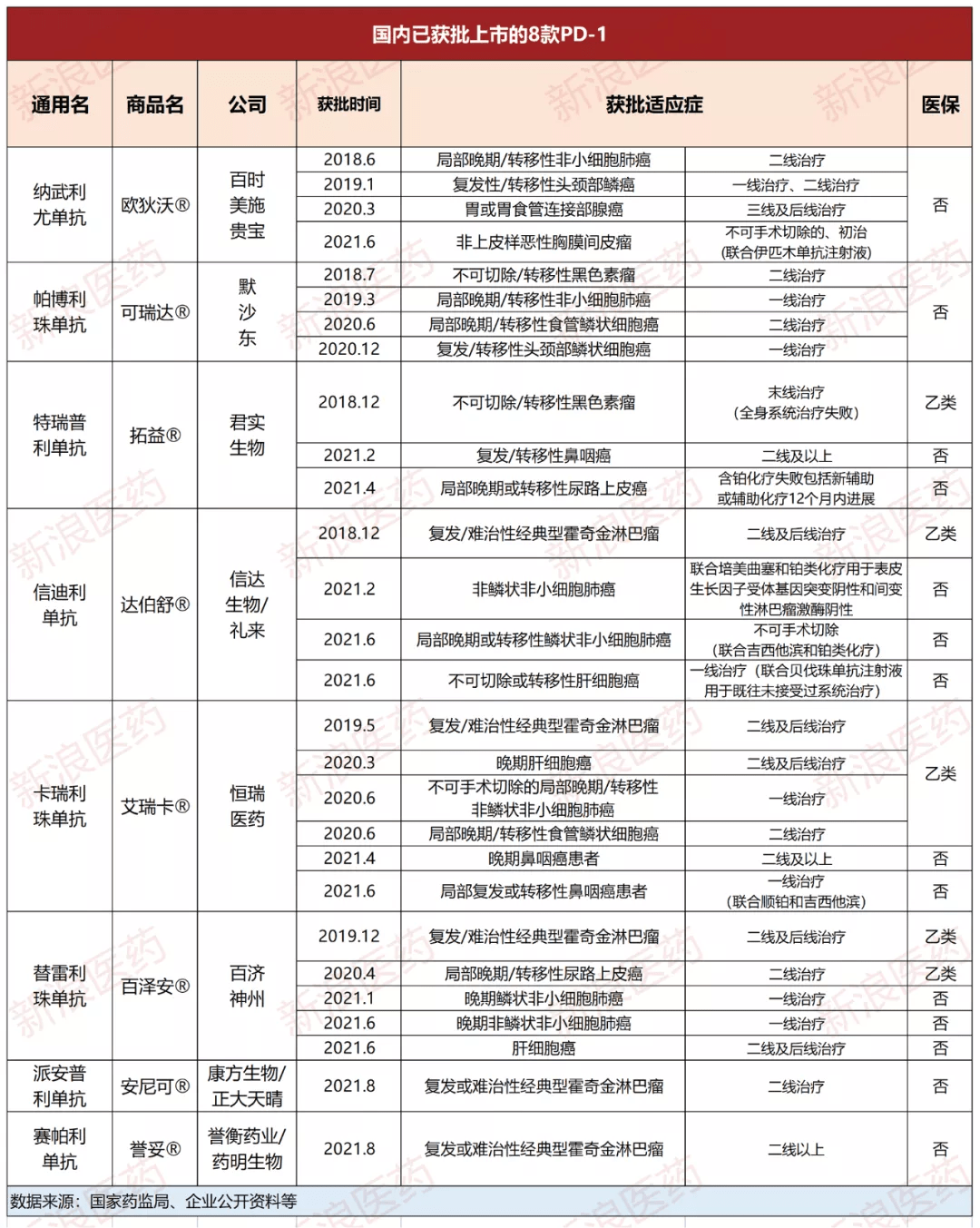
+△+ 君实生物去年亏损超22亿,核心品种加速“出海”,对冲国产PD-1内卷特瑞普利单抗于2018年12月获得国家药监局批准上市,是我国批准上市的首个国产以PD-1为靶点的单抗药物。2023年12月,特瑞普利单抗获得... 的靶向PD-1抑制剂药品。但整体来说,眼下中国PD-1市场已然是一片“红海”。更多获批时间偏晚的PD-1产品,只能在末位市场中夹缝求生,有...

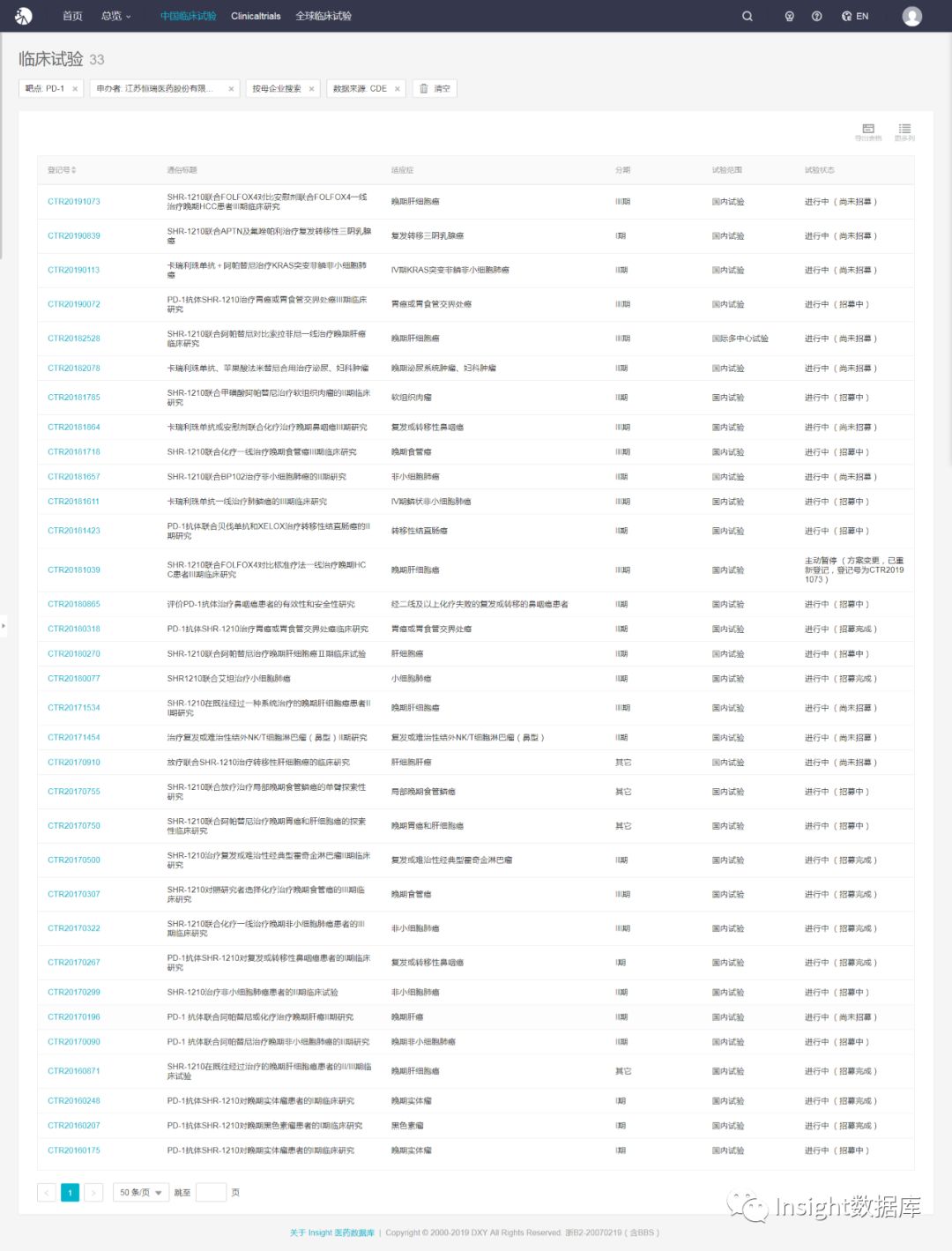
恒瑞医药卡瑞利珠单抗联用治疗肝细胞癌签署海外授权协议10月17日,恒瑞医药宣布,将公司自主研发的1类新药、PD-1抑制剂卡瑞利珠单抗(商品名:艾瑞卡®)与Rivoceranib(国内上市产品名称为阿帕替尼,商品名:艾坦®)联合用于治疗肝细胞癌(“联合疗法”)在除大中华区和韩国以外全球范围内开发及商业化的独家权利有偿许可给美国Elevar The...
o(?""?o 出海新进展!恒瑞创新药卡瑞利珠单抗联用治疗肝细胞癌签署海外授权10月17日,恒瑞医药宣布,将公司自主研发的1类新药、PD-1抑制剂卡瑞利珠单抗(商品名:艾瑞卡®)与Rivoceranib(国内上市产品名称为阿帕替尼,商品名:艾坦®)联合用于治疗肝细胞癌(“联合疗法”)在除大中华区和韩国以外全球范围内开发及商业化的独家权利有偿许可给美国Elevar The...

∪^∪ 奥赛康:子公司生物创新药ASKB589注册性临床III期研究完成中国首例...标志着国际范围内首个针对胃癌及食管胃交界处腺癌患者一线治疗的三联疗法(抗CLDN 18.2抗体联合化疗及PD-1抑制剂)的注册性临床研究全面启动。截至本公告披露之日,国内外尚无同靶点药物获批上市。本文源自中国财富通
18A药企生死劫,嘉和生物抗癌新药上市被拒,高瓴资本也踩坑嘉和生物在一众明星资本的“众星捧月”中上市,并且几乎同时提交了大单品PD-1抑制剂杰诺单抗的上市申请,开局颇佳。但令嘉和生物和高瓴资本想不到的是,历时近3年,杰诺单抗的上市申请最终被拒。而在这3年间,中国的PD-1市场早已发生了翻天覆地的变化。嘉和生物的股价也一路...
飞兔加速器部分文章、数据、图片来自互联网,一切版权均归源网站或源作者所有。
如果侵犯了你的权益请来信告知删除。邮箱:xxxxxxx@qq.com
上一篇:国内上市的pd-1有哪些
下一篇:国内上市的pd-1的价格





